Wer mehrere Medizinprodukte in summativen Usability Evaluationen bzw. Human Factors Validations validieren lassen will, steht oft vor folgendem Problem: diese Studien kosten jede Menge Zeit, Geld und andere Ressourcen.
Die Lösung kann in vielen Fällen heißen: Man kombiniert die Studien von mehreren Medizinprodukten. Unter welchen Voraussetzungen und wie genau das funktioniert, erfahren Sie hier in diesem Artikel.
Viel Spaß beim Lesen!
Ein Hinweis, bevor es losgeht
Der Begriff „Kombinierte Usability Studies“ ist kein Teil der Standards und Normen. Er stammt von uns und ist unser bewährter Lösungsvorschlag zur pragmatischen Umsetzung der verpflichtenden summativen Evaluation bzw. Human Factors Validations für mehrere Medizinprodukte.
Was ist eine Kombinierte Usability Study?
Eine abschließende und bewertende Usability Studie, in der mehrere Medizinprodukte zusammen oder nacheinander getestet werden, um zu zeigen, dass die Nutzung der Produkte frei von unakzeptablen Risiken abläuft.
Produkte, deren Usability Studien kombiniert werden können, könnten in diesem Kontext folgende sein:
- Zwei sehr ähnliche Medizinprodukte
- Ein Medizinprodukt und dazugehörige weitere Produkte
- Ein Medizinprodukt und die dazugehörige Software
Wann kann ich eine kombinierte Studie durchführen?
Die abschließende Validierung von mehreren Medizinprodukten kann in bestimmten Fällen kombiniert werden, insbesondere wenn die Produkte ähnliche Eigenschaften oder Anforderungen haben. Hier sind einige Schlüsselfaktoren, die berücksichtigt werden sollten:
- Ähnlichkeit der Produkte: Wenn die Medizinprodukte ähnliche Verwendungszwecke haben, kann es möglich sein, die Validierung zu kombinieren. Dies ist besonders relevant, wenn sie ähnliche Risikoprofile und Qualitätsanforderungen aufweisen.
- Gleichartige Testanforderungen: Wenn die Produkte denselben oder sehr ähnliche Tests zur Bestätigung ihrer Sicherheit und Wirksamkeit erfordern, kann eine kombinierte Validierung effizienter sein.
- Gleiche Nutzergruppe: Haben Sie mehrere Produkte mit gleichen oder sehr ähnlichen Nutzern, können Sie hier die Studien kombinieren.
Was sollten Sie zudem beachten?
Besonders beachten sollten Sie:
- Risikomanagement: Die Risikobewertung sollte für jedes Produkt individuell sowie für die Gruppe der Produkte insgesamt durchgeführt werden. Dies stellt sicher, dass alle spezifischen Risiken angemessen adressiert werden.
- Dokumentation und Nachverfolgbarkeit: Eine gründliche Dokumentation ist entscheidend, um die Validität und Nachvollziehbarkeit der Testergebnisse zu gewährleisten. Bei einer kombinierten Validierung muss klar sein, welche Daten zu welchem Produkt gehören.
- Safety first: Die Kombination von Validierungen kann kosteneffizient sein, aber es muss sichergestellt werden, dass dies nicht zu Kompromissen bei der Sicherheit oder Wirksamkeit der Produkte führt.
In der Praxis sollte die Entscheidung, ob eine kombinierte Validierung durchgeführt wird, auf einer gründlichen Bewertung der oben genannten Faktoren basieren und unter Einhaltung aller relevanten regulatorischen Anforderungen erfolgen. Es ist auch ratsam, bei Unklarheiten oder in komplexen Fällen eine Beratung durch Fachleute oder regulatorische Behörden in Anspruch zu nehmen.
Ein Beispiel für eine kombinierte Usability Studie
Für dieses Beispiel ist folgende Grundlage gegeben: Sie haben zwei Medizinprodukte, die von derselben vorgesehenen Nutzergruppe genutzt werden sollen. Sie entscheiden sich also, Ressourcen zu sparen, indem Sie:
- Einmalig eine simulierte Nutzungsumgebung aufbauen und ein Usability Labor vorbereiten
- Nur einmal Nutzer rekrutieren
- Ihr Team, das für die Durchführung verantwortlich ist, nur einmal schulen
So kann beispielsweise der Ablauf einer kombinierten Usability Studie für zwei Produkte mit der gleichen Nutzergruppe aussehen:
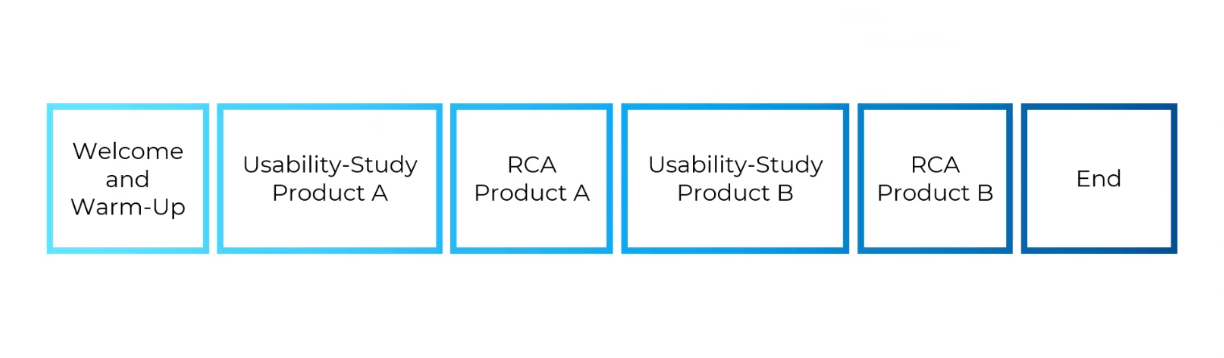
- Sie heißen den Teilnehmer willkommen und holen sich alle unterschriebenen Unterlagen zum Datenschutz ein
- Sie führen die Usability Studiey zu Produkt 1 durch
- Es folgt die Root Cause Analyse zu Produkt 1
- Dann fahren Sie mit der Usability Studie zu Produkt 2 fort
- Darauf folgt dann die Root Cause Analyse zu Produkt 2
- Am Ende verabschieden Sie Ihren Teilnehmer
Das sind alles natürlich nur Beispiele. Natürlich gibt es noch viele weitere Möglichkeiten. Diese alle aufzuzählen würde hier allerdings den Rahmen sprengen.
Sie wollen mehr erfahren?
Dann finden Sie hier unsere FAQ zum Thema. Wir haben Ihnen die 7 wichtigsten Fragen rund um das Thema beantwortet.
Fazit
Wo immer Sie Studien sinnvoll kombinieren können, sollten Sie genau das tun. Es gibt viele verschiedene Möglichkeiten eine kombinierte Usability- Studie durchzuführen.
Sie wollen wissen, ob sich eine kombinierte Studie in Ihrem Fall lohnt? Lassen Sie es uns gemeinsam herausfinden! Melden Sie sich über unser Kontaktformular. Wir freuen uns auf Sie.